 Содержание урока: Природные смеси веществ: природный газ, нефть, природные воды, минералы, воздух. Массовая доля компонента в смеси. Физические свойства веществ. Сохранение свойств веществ в смесях. Лабораторная работа «Изучение физических свойств железа, серы и их смеси».
Содержание урока: Природные смеси веществ: природный газ, нефть, природные воды, минералы, воздух. Массовая доля компонента в смеси. Физические свойства веществ. Сохранение свойств веществ в смесях. Лабораторная работа «Изучение физических свойств железа, серы и их смеси».
Цели урока: Организовать деятельность учащихся по изучению и первичному закреплению понятий «чистое вещество», «смесь веществ», «массовая доля компонента в смеси».
Помочь осознать учащимся практическую значимость учебного материала данной темы.
Обеспечить развитие у учащихся умений классифицировать смеси.
Содействовать развитию у школьников научных методов познания (наблюдение, эксперимент), химически правильной речи.
Требования к уровню подготовки учащихся:
Уметь:
* характеризовать состав смесей веществ;
* различать чистые вещества и смеси;
* обращаться с химической посудой и лабораторным оборудованием;
* вычислять массовую долю вещества в смеси.
* использовать приобретенные знания и умения в практической деятельности и повседневной жизни для: безопасного обращения с веществами и материалами.
Оборудование: прибор для опытов с электрическим током, 2 химических стакана на 150 мл, 2 химических стакана на 100 мл, магнит, воронка, фильтр, стеклянная палочка.
Реактивы и материалы: вода дистиллированная, раствор хлорида натрия, железо (опилки), сера (порошок), загрязненная соль, гранит, железный колчедан, геленит, сфалерит.
Ход урока:
1. Организационный момент.
2. Проверка домашнего задания.
а) что изучает химия?
б) что называют веществом?
в) на какие группы по составу можно разделить все вещества?
г) какие вещества называют простыми?
д) приведите примеры простых веществ.
е) какие вещества называют сложными?
ж) приведите примеры сложных веществ?
3. Изучение нового материала.
Сегодня мы поговорим о так называемых чистых веществах и смесях веществ.
Мы живем в мире веществ. Этот мир также многообразен и уникален, как и мир людей. В окружающем нас мире большинство материалов представляют собой смеси различных веществ. Так, большинство горных пород и многие минералы являются смесями.
Демонстрация 1. Образцы минералов (железный колчедан, гранит, галенит, сфалерит). Фотография киновари.
Наша пища и живые организмы, использующие природу как арену для своей деятельности (и часто сами являющиеся пищей для других живых организмов), представляют собой чрезвычайно сложные смеси органических соединений. Вкус апельсина, например, обусловлен присутствием сотен различных веществ.
Вода, железо, сахар представляют собой чистые вещества. Каждое из них характеризуется определенными свойствами: температурой плавления, плотностью, способностью вступать в определенные химические реакции.
Чистое вещество состоит из частиц одного вида и имеет постоянный состав, который может быть выражен единственной химической формулой. Например, вода в чистом виде состоит только из молекул Н2О, имеет определенные физические свойства. Вода в природе никогда не бывает чистой. Вследствие растворения различных веществ, природная вода всегда содержит примеси. Вспомните накипь на чайнике, откуда она появилась? Вещества, содержащиеся в растворенном виде в воде, при нагревании осаждаются на стенках посуды. Чтобы изучать свойства воды необходимо использовать только специальным образом очищенную воду. В лаборатории используют только так называемую дистиллированную воду, которая была получена перегонкой природной воды.
Задание: опишите физические свойства воды по плану (агрегатное состояние, цвет, запах, температура плавления, температура кипения, плотность, электропроводность, теплопроводность).
Способна ли чистая вода проводить электрический ток?
Демонстрация 2. Электропроводность дистиллированной и минеральной воды.
Почему мы получили разный результат при проведении этого эксперимента? Минеральная вода содержит растворенные вещества. Рассмотрите этикетки бутилированых минеральных вод. На них всегда указывается общая минерализация (масса растворенных веществ в 1 литре воды). Именно эти вещества и вызывают свечение электрической лампы при пропускании тока через минеральную воду.
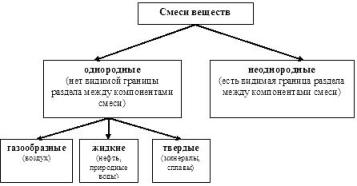 Рассмотрим, к примеру две смеси: сахар – вода и мел – вода. Первая смесь представляет прозрачную жидкость, внешне напоминающую воду. Данная смесь является однородной (или гомогенной). Другая смесь (мел – вода) не является однородной: она представляет собой крупинки мела, плавающие в воде. В смеси можно выделить малый объем, содержащий только твердое вещество или только жидкость, отличающиеся по свойствам. Если смесь оставить на некоторое время в покое, то произойдет разделение компонентов: мел выпадает в осадок, сверху будет слой чистой воды. Такие смеси называют гетерогенными.
Рассмотрим, к примеру две смеси: сахар – вода и мел – вода. Первая смесь представляет прозрачную жидкость, внешне напоминающую воду. Данная смесь является однородной (или гомогенной). Другая смесь (мел – вода) не является однородной: она представляет собой крупинки мела, плавающие в воде. В смеси можно выделить малый объем, содержащий только твердое вещество или только жидкость, отличающиеся по свойствам. Если смесь оставить на некоторое время в покое, то произойдет разделение компонентов: мел выпадает в осадок, сверху будет слой чистой воды. Такие смеси называют гетерогенными.
Состав смесей устанавливают с помощью химического анализа. При этом определяются концентрации веществ, составляющих смесь, в процентах или долях единицы. Для твердых и жидких смесей определяют, как правило, массовые доли (w), а для газообразных – объемные доли (y) веществ:
Например, объемная доля кислорода в воздухе равна 21% или в долях единицы – 0,21.
Задание: вычислите массовую долю растворенных веществ в минеральной воде. Массу одного литра воды примите равной 1 кг.
Сохраняют ли вещества в смесях свои свойства? Чтобы ответить на этот вопрос выполним лабораторную работу.
ЛАБОРАТОРНАЯ РАБОТА
Изучение свойств железа, серы и их смеси.
Цель: экспериментально выяснить изменяются ли свойства веществ после их смешивания.
Задание. В вашем распоряжении имеются: вода, порошки железа и серы, химический стакан, магнит, лист бумаги, шпатели.
С помощью шпателя поместите небольшие порции каждого вещества на лист бумаги отдельными кучками. Опишите физические свойства железа и серы по плану:
1. Агрегатное состояние.
2. Цвет.
3. Температура плавления (данные возьмите из справочника).
4. Температура кипения (данные возьмите из справочника).
5. Плотность (данные возьмите из справочника).
6. Особые свойства.
Смешайте стеклянной палочкой оба порошка на бумаге. Исследуйте отношение смеси к воде и магниту.
Результат вашей работы оформите в виде сравнительной таблицы.
| Железо | Сера | Смесь железа и серы | |
| Отношение к магниту | |||
| Отношение к воде |
Сделайте вывод по итогам работы: измелись ли свойства веществ (железа и серы) после их смешивания.
Домашнее задание. Прочитать материал учебника § 23, выполнить упражнения 1–4.









