 Цели урока:
Цели урока:
Создать условия для актуализации имеющихся у учащихся знаний об атомах, молекулах.
Организовать деятельность учащихся по первичному ознакомлению с понятием «химический элемент» и Периодической системой химических элементов.
Содействовать развитию у учащихся исследовательских умений в процессе поиска и анализа информации.
Требования к уровню подготовки учащихся:
Знать химическую символику: знаки химических элементов;
Уметь называть: химические элементы;
определять: состав веществ по их формулам.
Оборудование: ПСХЭ, таблица «Формы существования химических элементов», шаростержневая модель молекулы воды, модель кристаллической решетки железа, мультимедийный компьютер, проектор.
Ход урока:
1. Организационный момент.
2. Актуализация знаний учащихся.
1) Что изучает химия?
2) Что называют веществом?
3) Чем разные вещества отличаются друг от друга?
3. Постановка целей и задач урока.
Сегодня мы определим причину, по которой разные вещества имеют разные свойства.
Вы уже знаете, что вещества состоят из молекул, а молекулы – из атомов. О составе и строении вещества люди задумались очень давно. Предположение о существовании каких-то неделимых частиц, из которых состоят все вещества появилось в Древней Греции в работах философов Демокрита и Левкипта. Они рассуждали следующим образом: если взять какую-то порцию вещества и разделить ее пополам, а затем продолжить такое деление с вновь образующейся половинкой, то, в конце концов, останется такая порция вещества, которую уже не удастся разделить пополам. Именно эту порцию вещества они и предложили называть атомом (по-гречески атом – неделимый). К сожалению представления древнегреческих ученых, их гениальные догадки не получили распространения и признания. Уровень человеческих знаний в те времена не позволял признать «атом».
Об атомах вспомнили значительно позже, в период зарождения естественных наук. В XVII веке Роберт Бойль утверждал, что все химические превращения – результат соединении и разъединения атомов. Он ввел в науку понятие о химическом элементе как составной части вещества.
Демонстрация: Слайд «Роберт Бойль».
Наиболее последовательным приверженцем идеи атомизма в XVIII веке был великий русский ученый М.В.Ломоносов, в работах которого были заложены основы атомно-молекулярного учения.
Демонстрация: Слайд «Атомно-молекулярное учение».
Основные положения АМУ:
1. Вещества состоят из молекул.
2. Молекулы состоят из атомов.
3. Атомы представляют собой мельчайшие, химически неделимые частицы, из которых состоят молекулы.
Например, молекула воды состоит из двух атомов водорода и одного атома кислорода.
Демонстрация: Шаростержневая модель молекулы воды.
Металлы не имеют молекул, все они состоят только из отдельных атомов.
Демонстрация: Модель кристаллической решетки железа.
В последствии оказалось, что и атомы не являются неделимыми частицами. Таким образом в положения атомно-молекулярного учения были внесены поправки.
Демонстрация: Слайд «Поправки к атомно-молекулярному учению».
Джон Дальтон связал понятие о химическом элементе с атомной гипотезой о строении вещества. Именно он определил химический элемент как определенный вид атомов.
Демонстрация: Слайд «Джон Дальтон».
В настоящее время существует более строгое определение этого понятия с которым мы познакомимся позднее, а сейчас процитируем отрывок из стихотворения поэта Степана Щипачева «Читая Менделеева»:
«Другого ничего в природе нет
Ни здесь, ни там, в космических глубинах:
Все – от песчинок малых до планет –
Из элементов состоит единых …»
Демонстрация: Слайд «С.Щипачев «Читая Менделеева».
Давайте попробуем проанализировать этот отрывок. О чем в нем говорится?
1). Вся природа (живая и неживая) едина.
2). Все тела и следовательно вещества состоят из элементов.
Но что такое элемент? В толковом словаре можно прочитать, что «элемент – составная часть чего–либо».
Одним из величайших достижений химии было доказательство того факта, что все предметы в мире, будь то обломок скалы, капля воды, куриное перо или дерево, построены из химических элементов. К химическим элементам относят, например, кислород, водород, алюминий, медь, железо. Их назвали элементами по той причине, что их нельзя разложить на более простые вещества путем нагревания, высушивания, кипячения, обработкой кислотами или любым другим способом, которые применяют химики для превращения веществ. В настоящее время известно 111 химических элементов, из них существуют в природе 89, а остальные получены искусственно. Поразительно, как из такого ограниченного набора нитей природе удалось соткать богатый ковер мира.
Каждый химический элемент имеет свое название и обозначается особым знаком – символом. В качестве символов, по предложению шведского химика Й. Берцелиуса, были приняты первые или первая и последующая буквы латинских названий химических элементов.
Демонстрация: Слайд «Й.Я.Берцелиус».
Например, химический элемент водород (латинское название Hydrogenium) имеет символ Н, кислород (латинское название Oxygenium) – O, сера (латинское название Sulfur) – S. Существует много химических элементов, латинские названия которых начинаются с одной буквы. В этом случае берут первую и одну из последующих букв. Например, кремний (Silicium) – Si, олово (Stannum) – Sn, кальций (Calcium) – Ca, медь (Cuprum) – Cu, хлор (Chlorum) – Cl.
Названия химических элементов указывают на свойства веществ, географические объекты, планеты солнечной системы, имена выдающихся ученых.
| Признак названия | Химические элементы |
| Свойства веществ | Водород – рождающий воду Кислород – рождающий кислоты Фосфор – несущий свет Азот – безжизненный Фтор – разрушающий Бром – зловонный Иод – фиолетовый |
| Названия планет | Селен – Луна Теллур – Земля Уран Плутоний Нептуний |
| Географические названия | Ge – Германия Ga – Франция Po – Польша Sc – Fr – Франция Ru – Россия Eu – Европа Am – Америка |
| Имена ученых | Cm – Кюрий Fm – Фермий Es – Эйнштейн Md – Менделеев Lr – Лоуренс |
Все химические элементы объединены в Периодическую систему элементов, составленную великим русским химиком Д.И.Менделеевым. Каждый элемент в Периодической системе имеет свой номер.
Демонстрация: Слайд «Структура периодической системы»
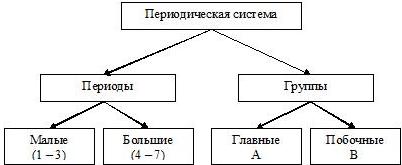
В результате работ многих ученых изменилось и содержание понятий «атом» и «молекула».
|
Атом – наименьшая частица химического элемента, носитель его свойств.
|
Каждому химическому элементу соответствует совокупность определенных атомов. Связываясь друг с другом, атомы одного или разных элементов образуют более сложные частицы, например молекулы. Все многообразие веществ (твердых, жидких и газообразных) обусловлено различными сочетаниями атомов между собой.
| Молекула – частица вещества, которая образована из двух или более атомов и способна к самостоятельному существованию. |
Атомы могут существовать в свободном состоянии, в составе простых и сложных веществ.
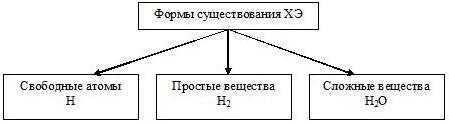
| Простое вещество – вещество, образованное атомами одного химического элемента. |
| Сложное вещество – вещество, образованное атомами разных химических элементов |
Д.з. § 4, записать определения в словарь, выучить символы х.э., упр.5.









